二甲醚(DME)是一种绿色的替代能源, 燃烧清洁, 原料来源丰富, 具有良好的应用前景[1]。二甲醚的汽化及燃烧特性类似天然气, 可以作为燃料使用[2]。由于其十六烷值高, 也可以作为柴油添加剂[3]。另外, 二甲醚的毒性低, 可以替代氟利昂作为气雾剂和制冷剂[4]。同时, 还可以用于制备低碳烯烃等产品[5], 是一种优良的化工原料。二甲醚的制备方法有一步法和两步法。工业上应用比较多的是两步法, 即先用合成气制备甲醇, 然后甲醇脱水制备二甲醚。这种方法的缺点是受甲醇合成反应转化率的限制, 原料单程转化率不高。目前研究较多、比较有发展前途的是一步法合成二甲醚[6-7]。即在一个反应器中同时完成甲醇合成与甲醇脱水两个反应, 直接得到二甲醚。由于反应间存在协同效应, 打破了反应平衡的限制, 使原料单程转化率大幅提高[8-9]。一步法合成二甲醚的催化剂失活较快, 其原因是由甲醇合成组分的失活引起。影响失活的因素有铜组分的烧结[10]、铜组分的流失[11]和积碳[12]等。由于一步法合成二甲醚采用的是双功能催化剂, 甲醇合成与甲醇脱水组分间存在协同效应, 因此催化剂的寿命会受到协同作用的影响。笔者考察协同效应不同的催化剂的失活情况, 研究催化剂间的协同效应对催化剂寿命的影响, 探讨催化剂的失活原因。
1 实验 1.1 实验药品和仪器实验用原料气由H2和CO钢瓶提供。甲醇合成催化剂选用西南化工研究院的XNC-98催化剂, 主要成分为CuO-ZnO-Al2O3。甲醇脱水催化剂选用上海恒业分子筛厂生产的HZSM-5分子筛催化剂, 硅铝比分别为40和75。
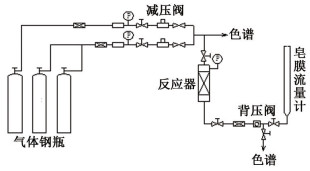
催化剂活性及稳定性实验装置如图 1。反应原料气来源于气体钢瓶, 用质量流量计控制各路气体的流量以配制不同浓度的原料气。反应在微型不锈钢固定床反应器中进行, 反应器外有电阻丝进行加热, 用热电偶控制反应温度。采用皂膜流量计测量反应尾气量。产物采用上海天美公司的7890T气相色谱仪在线取样分析, 用色谱自带的T2000P软件进行数据处理。催化剂的的比表面积、孔容和孔径分布在美国Micromeritics公司生产的ASAP2010比表面测定仪上进行测试, 使用的方法为N2吸附脱附。使用日本理学Rigaku D/max 2550 VB/PC型X射线衍射仪对样品进行XRD测试, Cu靶, Ka射线, 管电压40 kV, 管电流100 mA, 扫描速度8(°)/min, 扫描范围2θ=0°~80°。采用自制设备进行催化剂的氨吸附脱附实验, 以检测催化剂表面的强酸与弱酸中心的数量。催化剂热重分析(TGA)在美国TA公司的SDT Q600设备上进行, 样品置于瓷舟中, 在N2气氛下由室温以10 ℃/min的升温速率加热到600 ℃, 用热重天平记录失重情况。
|
图 1 固定床实验装置 Fig.1 Diagram of fixed-bed reactor |
将甲醇合成组分XNC-98与甲醇脱水组分HZSM-5破碎成10 μm以下的粉末, 采用两种方法制备复合催化剂, 催化剂中XNC-98与HZSM-5的质量配比从2:1至6:1。一种是将两种催化剂粉末按比例混合均匀, 在压片机中压片成型, 再破碎、筛分至0.042~0.084 mm进行实验, 制备的催化剂命名为cat1;另一种方法为分别将XNC-98催化剂与HZSM-5催化剂压片、破碎、筛分至0.042~0.084 mm, 然后将两种催化剂按比例混合好进行实验, 制备的催化剂命名为cat2。
1.3 催化剂还原方法采用两种不同的还原方法, 以考察还原条件对催化剂寿命的影响。
还原方法1:纯氢气进行还原。催化剂置于固定床反应器中, 以100 mL/min的速率通入H2, 同时以1 ℃/min的升温速率从室温升至230 ℃后恒温4 h, 还原完毕。整个还原时间约需8 h。
还原方法2:用H2与N2配制还原气体, 还原气中的H2含量逐渐增加, 最高不超过15%。还原气流量为100 mL/min, 最高还原温度仍为230 ℃。整个还原时间约20 h。
1.4 催化剂活性及稳定性实验催化剂还原完毕后, 切换还原气为CO/H2=1:1(体积比)的原料气进行反应。反应温度220~260 ℃, 反应压力3 MPa, 空速3000 mL/(g·h)。进行催化剂寿命实验时, 反应条件与上述相同, 每12 h记录一次数据, 并计算CO转化率及二甲醚选择性, 总实验时间为250~300 h。
CO转化率及DME收率与选择性的计算公式为
| $ {x_{{\rm{CO}}}} = \frac{{{F_{{\rm{in}}}}{y_{{\rm{CO, in}}}}-{F_{{\rm{out}}}}{y_{{\rm{CO, out}}}}}}{{{F_{{\rm{in}}}}{y_{{\rm{CO, in}}}}}}{\rm{, }} $ | (1) |
| $ {y_{{\rm{DME}}}} = \frac{{2{F_{{\rm{out}}}}{y_{{\rm{DME, out}}}}}}{{{F_{{\rm{in}}}}{y_{{\rm{CO, in}}}}}}, $ | (2) |
| $ {S_{{\rm{DME}}}} = \frac{{{y_{{\rm{DME}}}}}}{{{x_{{\rm{CO}}}}}}. $ | (3) |
式中, xCO为CO转化率; yDME为二甲醚收率; SDME为二甲醚选择性; Fin和Fout分别为原料气与尾气流量; yCO, in与yCO, out分别为原料气与尾气中CO体积分率; yDME, out为尾气中二甲醚体积分率。
2 结果分析 2.1 催化剂活性及适宜操作条件的确定一步法合成二甲醚由以下3个反应构成。
甲醇合成反应:
| $ {\rm{CO + 2}}{{\rm{H}}_{\rm{2}}} \Leftrightarrow {\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{OH}}{\rm{.}} $ | (4) |
甲醇脱水反应:
| $ {\rm{2C}}{{\rm{H}}_{\rm{3}}}{\rm{OH}} \Leftrightarrow {\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{OC}}{{\rm{H}}_{\rm{3}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}}. $ | (5) |
逆水汽变换反应:
| $ {\rm{CO + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} \Leftrightarrow {\rm{C}}{{\rm{O}}_{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{.}} $ | (6) |
甲醇脱水反应消耗了甲醇合成反应的产物, 逆水汽变换反应又消耗了甲醇脱水反应生成的水, 同时生成氢气, 为甲醇合成反应提供原料, 从而打破了反应平衡, 提高了CO转化率。这3个反应之间相互促进, 相互制约, 相互影响的关系就是协同效应。催化剂的制备过程、还原过程及反应条件均会对协同效应影响。
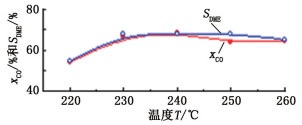
在催化剂配比XNC-98/HZSM-5为4的条件下, 反应温度从220 ℃升至260 ℃, 每10 ℃记录一次数据, 考察催化剂的性能, 结果见图 2。
|
图 2 温度对反应的影响 Fig.2 Effect of temperature on reaction |
由图 2可知, 反应温度在220~260℃范围内, CO转化率先升高后降低, 在240 ℃达到最高。说明反应的最佳温度为240 ℃。由于二甲醚合成反应为放热反应, 温度升高时, 反应速率也提高, 但反应平衡则向相反方向移动。在低温下, 反应受动力学控制, 升温则CO转化率和DME收率也升高; 在高温下反应时则相反, 反应受热力学平衡控制, 升温则转化率下降。滕丽华等[13]研究表明, 对一步法合成二甲醚复合催化剂而言, 低温有利于甲醇合成反应, 高温有利于甲醇脱水反应, 因此最佳反应温度也是催化剂协同效应的一种表现。
维持反应温度240 ℃, 反应压力3 MPa, 改变催化剂的配比, 考察不同组成催化剂的性能, 结果见表 1。
| 表 1 不同配比催化剂对反应的影响 Table 1 Effects of catalysts with different ratios on reaction |
由表 1可见, 两种组分配比在2:1~6:1范围内, CO转化率及DME收率变化不大, 说明两种组分在反应条件下活性均比较高, 因此可以在一个比较宽的范围内配合使用。比较而言, 当XNC-98/HZSM-5为4:1时, 复合催化剂的活性最高。说明此时两种催化剂间的协同效应最好。当催化剂复合比小于4时, 催化剂中HZSM-5所占比重较大, 生成的甲醇易脱水生成DME, 但由于甲醇合成组分含量相对少, 甲醇合成速率慢, 甲醇合成反应与甲醇脱水反应之间不能良好协同; 当复合比大于4时, 虽然催化剂中甲醇合成组分的含量提高, 甲醇合成速率加快, 但脱水反应速率下降, 也不利于反应间的协同效应; 而当催化剂复合比为4时, CO转化率及DME收率达最大值, 说明此时甲醇合成、甲醇脱水及水气变换三个反应达到良好协同。对于XNC-98和HZSM-5催化剂, 适宜的催化剂配比为4:1。
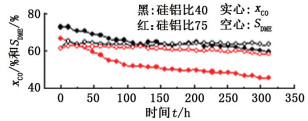
2.2 复合催化剂组成对协同效应及寿命的影响由于复合催化剂由甲醇合成与甲醇脱水两种组分构成, 因此选用硅铝比分别为40与75的分子筛与XNC-98甲醇合成催化剂组成复合催化剂, 在固定床反应器中进行催化剂稳定性实验, 以考察不同催化剂组成的影响。结果见图 3。
|
图 3 分子筛硅铝比对复合催化剂性能的影响 Fig.3 Effect of molecular sieve Si/Al ratio on properties of composite catalysts |
由图 3可知, 采用硅铝比为40的HZSM-5分子筛与XNC-98组成的复合催化剂, 初始活性高且CO转化率下降较慢, 说明无论从催化活性还是催化剂的稳定性上都比硅铝比为75的分子筛更好, 因此硅铝比为40的分子筛与XNC-98催化剂间的协同效应更强。
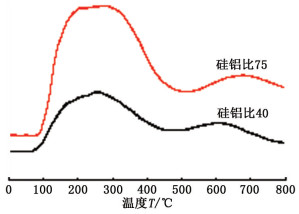
由于脱水催化剂采用的是HZSM-5分子筛, 而分子筛的脱水性能主要由其表面的酸性位控制, 为考察不同硅铝比分子筛催化性能上的差异, 对分子筛进行NH3-TPD研究, 谱图见图 4。
|
图 4 不同硅铝比分子筛的NH3-TPD图谱 Fig.4 NH3-TPD spectra of different silica alumina ratio molecular sieves |
由图 4看出, 硅铝比不同的分子筛上均存在两种酸强度中心, 即200~300 ℃所对应的弱酸中心和600~700 ℃所对应的强酸中心。从峰强度上可知, 弱酸中心的酸量均大于强酸中心的酸量。说明弱酸中心是催化剂的主要活性中心。Si/Al=75的分子筛其弱酸量和强酸量均大于Si/Al=40的分子筛, 但其复合催化剂活性较低。原因是尽管酸性位较多, 脱水反应的活性中心多, 但反应生成的水需要在甲醇合成催化剂上进行逆水汽变换反应, 而逆水汽变换反应速率较慢, 致使体系中含水量上升。水的存在一方面抑制了甲醇脱水反应的进行, 另一方面, 也使甲醇合成催化剂更易因Cu烧结而失活, 同时, 酸性中心多也使催化剂更易积碳, 同样造成催化剂失活速率加快。因此从反应的协同效应上来说, 硅铝比为40的分子筛与甲醇合成催化剂的配合更好, 反应活性与催化剂稳定性也更好。
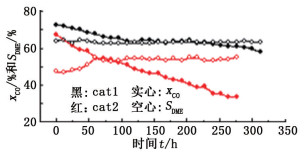
2.3 催化剂制备方法对寿命的影响不同的催化剂制备方法也会影响两种组分间的协同效应, 结果见图 5。
|
图 5 不同催化剂制备方法对催化剂寿命的影响 Fig.5 Effect of different catalyst preparation methods on catalyst life |
由图 5可知, 在反应进行300 h后, 两种催化剂均出现了不同程度的失活, 而且cat2的失活速率明显高于cat1。经计算, cat1的CO转化率下降速率为0.052%/h, 而cat2的为0.116%/h, 差别非常明显。这是由于两种催化剂在制备方法上存在差异, 协同效应上也不一样。cat1的每一个催化剂颗粒中既有甲醇合成组分, 也有甲醇脱水组分, 两种催化剂结合较为紧密, 协同效应较强; cat2的每一个催化剂颗粒中则只有一种组分, 催化剂间的结合较为疏松, 协同效应较弱。从实验结果可以看出, 协同效应强的催化剂的活性与稳定性都更好。
从二甲醚的选择性上看, 采用cat1的体系, 二甲醚选择性一直保持在65%左右, 说明催化剂的失活主要由甲醇合成催化剂造成; 而采用cat2的体系, 二甲醚选择性开始只有46%左右, 随反应进行至70 h以后保持在约55%。另外, 从CO转化率上也可以看出, cat2体系CO转化率在约70 h有一拐点, 下降速率减缓(72 h之前CO转化率下降速率为0.194%/h, 72 h之后变为0.093%/h), 说明催化剂的失活并非保持匀速, 而是随反应的进行发生了变化。表 2为采用两种不同方法制备的催化剂在不同反应时刻产物中水和甲醇的含量。可以看出, 刚开始反应时, 甲醇合成速率较快, 采用协同效应较弱的cat2时, 部分生成的甲醇与水没来得及转化就随反应物排出, 造成二甲醚的初始选择性较低, 同时体系中水与甲醇含量较高, 而较高的水含量也加速了甲醇合成催化剂的失活。反应进行一段时间后, 由于甲醇合成催化剂失活速率较快, 甲醇生成速率降低, 而甲醇脱水催化剂的活性下降较少, 生成的甲醇大部分在脱水催化剂上转化为二甲醚, 使二甲醚的选择性提高, 同时体系中的水含量与甲醇含量均降低, 催化剂失活速率下降。从图上看, 就出现了反应约70 h时CO转化率的一个拐点。
| 表 2 反应产物中H2O与甲醇的含量 Table 2 Content of H2O and methanol in reaction products |
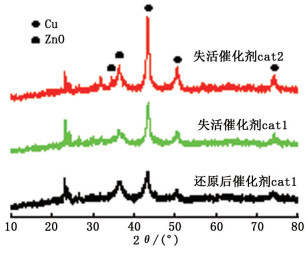
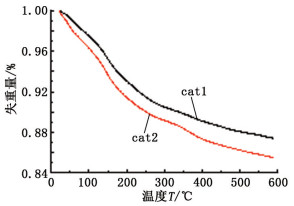
为分析失活后催化剂的体相特征, 找到催化剂失活原因, 对催化剂进行XRD分析, 结果如图 6所示。由于Cu催化剂有弱的C—C键断裂的能力[14], 同时, 脱水反应采用的是HZSM-5分子筛, 表面有较多酸性位, 有可能造成积碳。为考察积碳状况, 对失活后的催化剂作了热重(TGA)分析, 结果见图 7。
|
图 6 失活催化剂的XRD谱图 Fig.6 XRD spectra of deactivated catalysts |
|
图 7 失活后催化剂的热重分析 Fig.7 Thermogravimetric analysis of catalyst after deactivation |
从XRD谱图可以看出, 与刚还原的催化剂相比, 不论采用何种制备方法, 失活催化剂中Cu的特征峰(43.2°, 50.4°, 74.1°)都变得尖细, 说明催化剂中的Cu晶粒已有一定程度的烧结。
cat2则表现得尤为明显。经计算, 还原后反应前催化剂的Cu晶粒为8.4 nm, cat1失活后Cu晶粒为10.2 nm, 而cat2失活后Cu晶粒已变为15.6 nm。二者相比, 说明催化剂的协同效应对延缓甲醇合成催化剂中Cu晶粒的长大, 延长催化剂寿命有非常大的影响。
从热重曲线上看, 不论采用何种方法制备催化剂, 失活后的催化剂都有一定程度的失重, 说明失活后催化剂表面均有积碳。两种催化剂失重曲线的形状比较类似, 说明附着在催化剂表面的物质相同。升温至600 ℃后, cat2比cat1失重量大, 说明cat2催化剂表面的积碳量大于cat1。表明协同效应对催化剂表面的积炭量也有很大影响。
表 3为失活前后催化剂表面的BET分析结果。可以看出, 催化剂失活后, 其比表面积明显减小, 造成与反应物接触的活性中心减少, 从而使反应速率降低。比表面积减少的原因主要是甲醇合成催化剂中的Cu的烧结以及催化剂表面的积碳。
| 表 3 失活前后催化剂的BET分析 Table 3 BET analysis of catalysts before and after inactivation |
结合XRD、热重及BET的分析结果可知, 由于cat1比cat2催化剂间的协同效应强, 催化剂的活性及稳定性都较高, 而且催化剂中Cu的烧结情况与积炭量都好于cat2。说明协同作用可以有效地缓解Cu的烧结以及催化剂的结焦, 对延长催化剂的寿命有很好的效果。
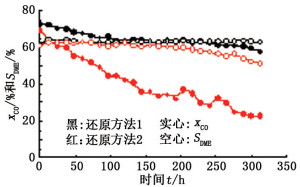
2.4 还原条件对催化剂协同效应及寿命的影响用不同的还原方法将催化剂还原后, 在固定床反应器中进行了催化剂寿命实验, 所使用的催化剂为cat1。实验结果见图 8。
|
图 8 不同还原方法对催化剂寿命的影响 Fig.8 Effect of different reduction methods on catalyst life |
从图 8看出, 在反应器中操作300 h后, 采用方法2还原的催化剂, CO转化率从72.8%下降为57.7%;而采用方法1还原的催化剂, CO转化率从69.4%下降到24.8%。比较可知, 不论是催化剂的初始活性还是失活速率, 采用方法2还原的催化剂都明显好于采用方法1还原的催化剂。说明催化剂的还原方法对协同效应及催化剂的稳定性都有影响。
为研究不同还原方法对催化剂协同效应的影响, 采用XRD对催化剂进行表征, 结果如图 9。
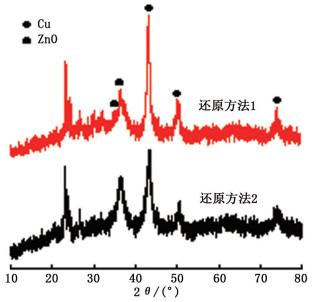
|
图 9 不同还原方法还原后催化剂的XRD谱图 Fig.9 XRD spectra of catalysts after different reduction methods |
由图 9可知, 尽管采用了不同的还原方法, 还原结束后, 催化剂中的CuO均被还原为Cu0(特征峰43.2°, 50.4°, 74.1°)。但从谱图中可以看出, 采用方法2还原的催化剂Cu0峰较为弥散, 说明Cu在催化剂中的分散程度比较好。而采用方法1还原的催化剂谱图中Cu峰较为尖细, 说明Cu已经有一定程度的烧结。从Cu晶粒来比较, 采用方法1还原的催化剂Cu晶粒为10.8 nm, 而采用方法2还原的催化剂Cu晶粒为8.4 nm, 可知采用方法2还原的催化剂Cu晶粒较小, 与脱水催化剂间的协同效应更强, 因此其活性和稳定性更高。
3 结论(1) 催化剂的组成、催化剂的制备方法以及催化剂的还原过程都会对催化剂的协同效应产生影响。
(2) 协同效应对催化剂的失活有较大影响, 协同效应强的催化剂失活速率较慢。
(3) 失活主要是由甲醇合成催化剂中的Cu组分烧结和积碳引起。
| [1] |
艾珍. 一步法合成二甲醚反应器的研究进展[J]. 化学工业与工程技术, 2010, 31(1): 15-17, 22. AI Zhen. Research development of reactor for one step synthesis of dimethyl ether from synthesis gas[J]. Journal of Chemical Industry & Engineering, 2010, 31(1): 15-17, 22. |
| [2] |
ZHANG L, HUANG Z. Life cycle study of coal-based dimethyl ether as vehicle fuel for urban bus in China[J]. Energy, 2007, 32(10): 1896-1904. DOI:10.1016/j.energy.2007.01.009 |
| [3] |
张正军, 尚乃名. 二甲醚产业发展前景探讨与展望[J]. 中氮肥, 2011(6): 1-4. ZHANG Zhengjun, SHANG Naiming. Prospect of dimethyl ether's industrialization[J]. M-Sized Nitrogenous Fertilizer Progress, 2011(6): 1-4. |
| [4] |
侯昭胤, 费金华, 郑小明. 二甲醚的应用和生产工艺[J]. 石油化工, 1999, 28(1): 59-61. HOU Zhaoyin, FEI Jinhua, ZHENG Xiaoming. Application and production process of DME[J]. Petrochemical Technology, 1999, 28(1): 59-61. |
| [5] |
徐瑶, 商永臣, 牛梦婷, 等. 二甲醚催化氧化制取甲缩醛[J]. 化学工程师, 2016, 245(2): 68-70. XU Yao, SHANG Yongchen, NIU Mengting, et al. Catalytic oxidation of dimethyl ether to dimethoxymethane[J]. Chemical Engineer, 2016, 245(2): 68-70. |
| [6] |
LU W Z, TENG L H, XIAO W D. Simulation and experiment study of dimethyl ether synthesis from syngas in a fluidized-bed reactor[J]. Chemical Engineering Science, 2004(59): 5455-5464. |
| [7] |
娄贺. 一步法制备二甲醚的催化剂研究[J]. 当代化工, 2016, 45(4): 847-849, 852. LOU He. Research on the catalyst for one-step preparation of dimethyl ether[J]. Contemporary Chemical Industry, 2016, 45(4): 847-849, 852. |
| [8] |
郑欢欢, 伍联营, 胡仰栋. 合成气一步法制备二甲醚的工艺流程模拟与优化[J]. 化工进展, 2013, 32(6): 1236-1241. ZHENG Huanhuan, WU Lianying, HU Yangdong. Process simulation and optimization of one-step synthesis of dimethyl ether from syngas[J]. Chemical 1ndustry and Engineering Progress, 2013, 32(6): 1236-1241. |
| [9] |
CHEN W H, HSU C L, WANG X D. Thermodynamic approach and comparison of two-step and single step DME (dimethyl ether) syntheses with carbon dioxide utilization[J]. Energy, 2016(109): 326-340. |
| [10] |
CARROLL M C, SKROTZKI B, KURTZ M, et al. Growth of copper particles in a Cu/ZnO methanol catalyst[J]. Scripta Materialia, 2003(49): 527-532. |
| [11] |
PENG X D, TOSELAND B A, UNDERWOOD R P. A novel mechanism of catalyst deactivation in liquid phase synthesis gas-to-DME reactions[J]. Studies in Surface Science and Catalysis, 1997(111): 175-182. |
| [12] |
AGUAYO A T, ERENA J, SIERRA J, et al. Deactivation and regeneration of hybrid catalysts in the single-step synthesis of dimethyl ether from syngas and CO2[J]. Catalyst Today, 2005, 106(1/2/3/4): 265-270. |
| [13] |
滕丽华, 鲁文质, 李霞, 等. 成二甲醚过程中的多功能催化协同效应[J]. 华东理工大学学报, 2004, 30(4): 365-369. TENG Lihua, LU Wenzhi, LI Xia, et al. Multifunctional catalytic synergy in the dimethyl ether synthesis process[J]. Journal of East China University of Science and Technology, 2004, 30(4): 365-369. |
| [14] |
王东升, 谭猗生, 韩怡卓, 等. 浆态床合成二甲醚复合催化剂失活原因探索[J]. 燃料化学学报, 2008, 36(2): 176-180. WANG Dongsheng, TAN Yisheng, HAN Yizhuo, et al. Study on deactivation of hybrid catalyst for dimethyl ether synthesis in slurry reactor[J]. Journal of Fuel Chemistry and Technology, 2008, 36(2): 176-180. |
 2017,
Vol. 41
2017,
Vol. 41